AI Jeneratörü için
Sınavlar, Fişler
& Daha
Sıkıcı çalışma içeriğinizi tek bir tıklamayla etkileşimli yapay zeka destekli çalışma kağıtlarına, sınavlara, bilgi kartlarına ve pratik sorulara dönüştürün. Başlamak için bugün PDF'leri, belgeleri, ses dosyalarını ve videoları yükleyin.
Manuel çalışmayı durdurun
Çoğu öğrenci verimsiz öğrenme yöntemlerine zaman harcıyor
Uzun belgelerinizi tekrar tekrar okumak veya saatlerce elle bilgi kartları ve özetler oluşturmak yerine, bu adımları atlamanıza yardımcı oluyoruz.
Bilgi içinde boğulmayı bırakın ve yapay zekamızın gerçekten önemli olanı filtrelemesine izin verin. Hızla kendinizi test etmeye başlayın ve daha hızlı gelişin.
Çok az kişi kişisel bir öğretmene para ayırabilir. StudyBlaze bunu sonsuza dek değiştirir. Etkileşimli öğrenme ilerlemenizi 10 kat daha hızlı hale getirir.
Çalışma materyallerini elle oluşturmak, kendinizi eğitmek ve test etmek için harcayabileceğiniz bir zamandır. Manuel çalışmayı tamamen ortadan kaldırarak stresi azaltın.
24/7 hizmet veren bir AI Öğretmeni
Her gün bir öğretmene erişin
Cevaplarınıza anında geri bildirim alın
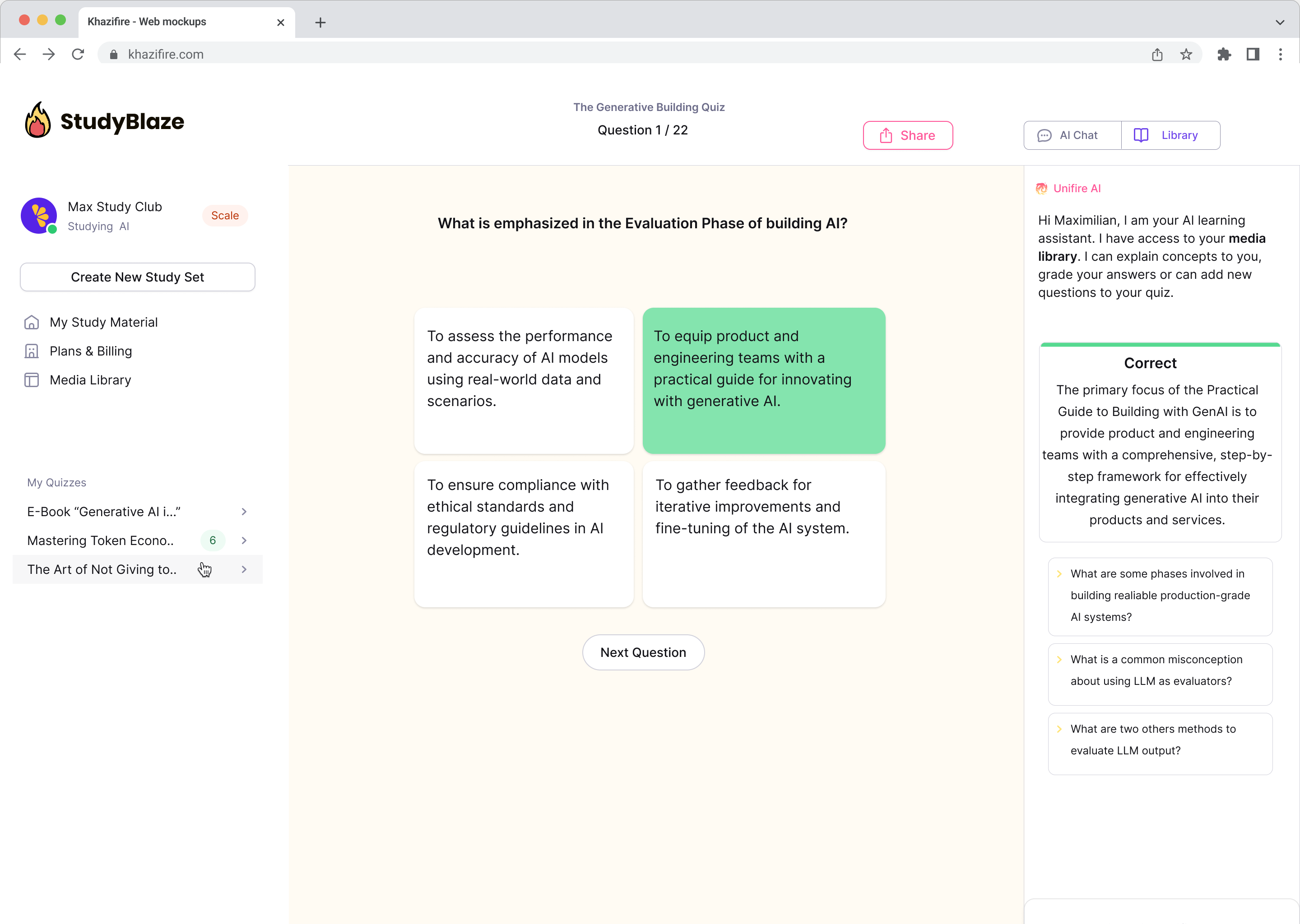
Belgelerinizle sohbet edin ve karmaşık konuları daha hızlı anlayın
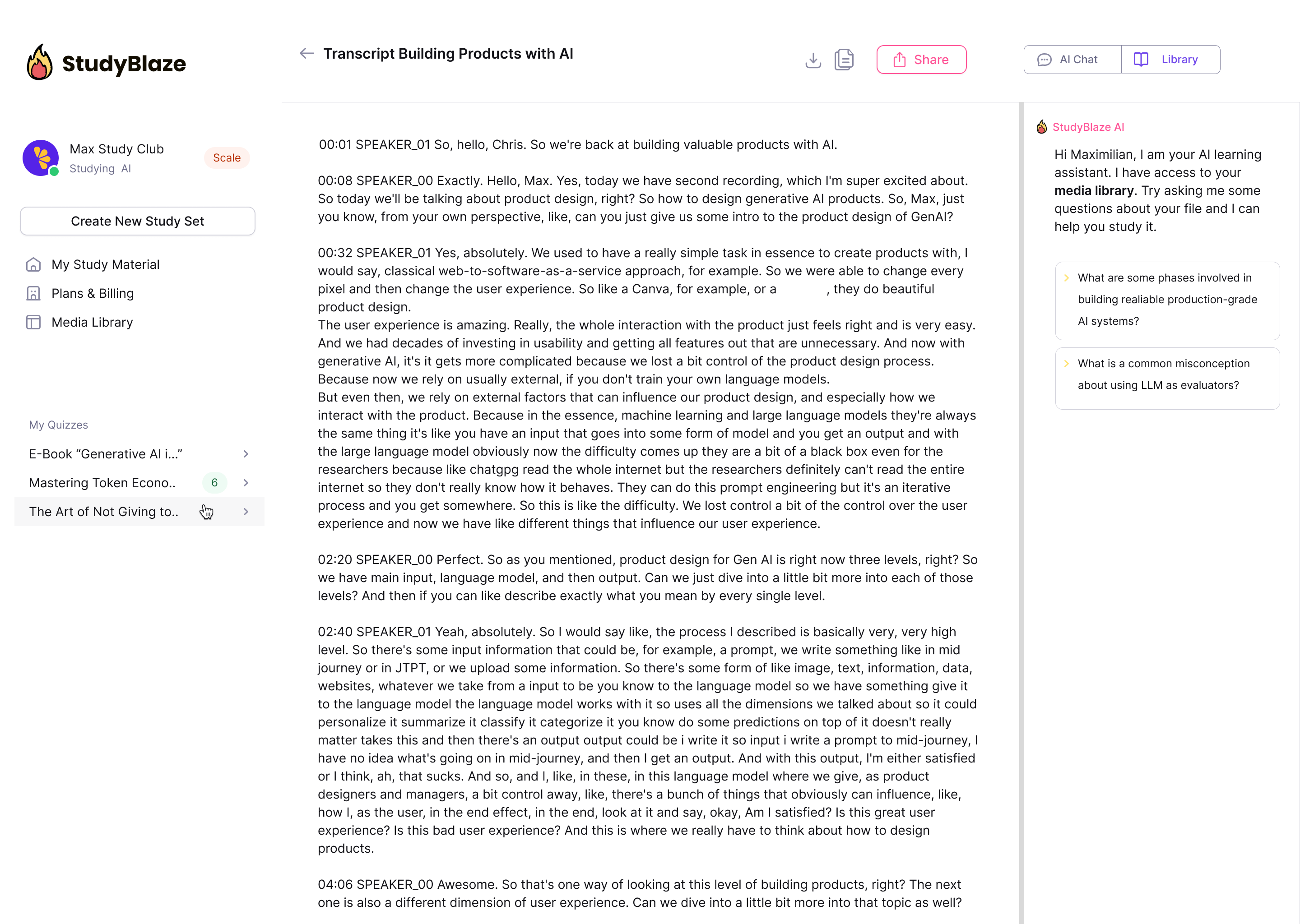
Yapay zeka eğitmeninizin cevaplarınızı derecelendirmesine ve neyi kaçırdığınızı söylemesine izin verin
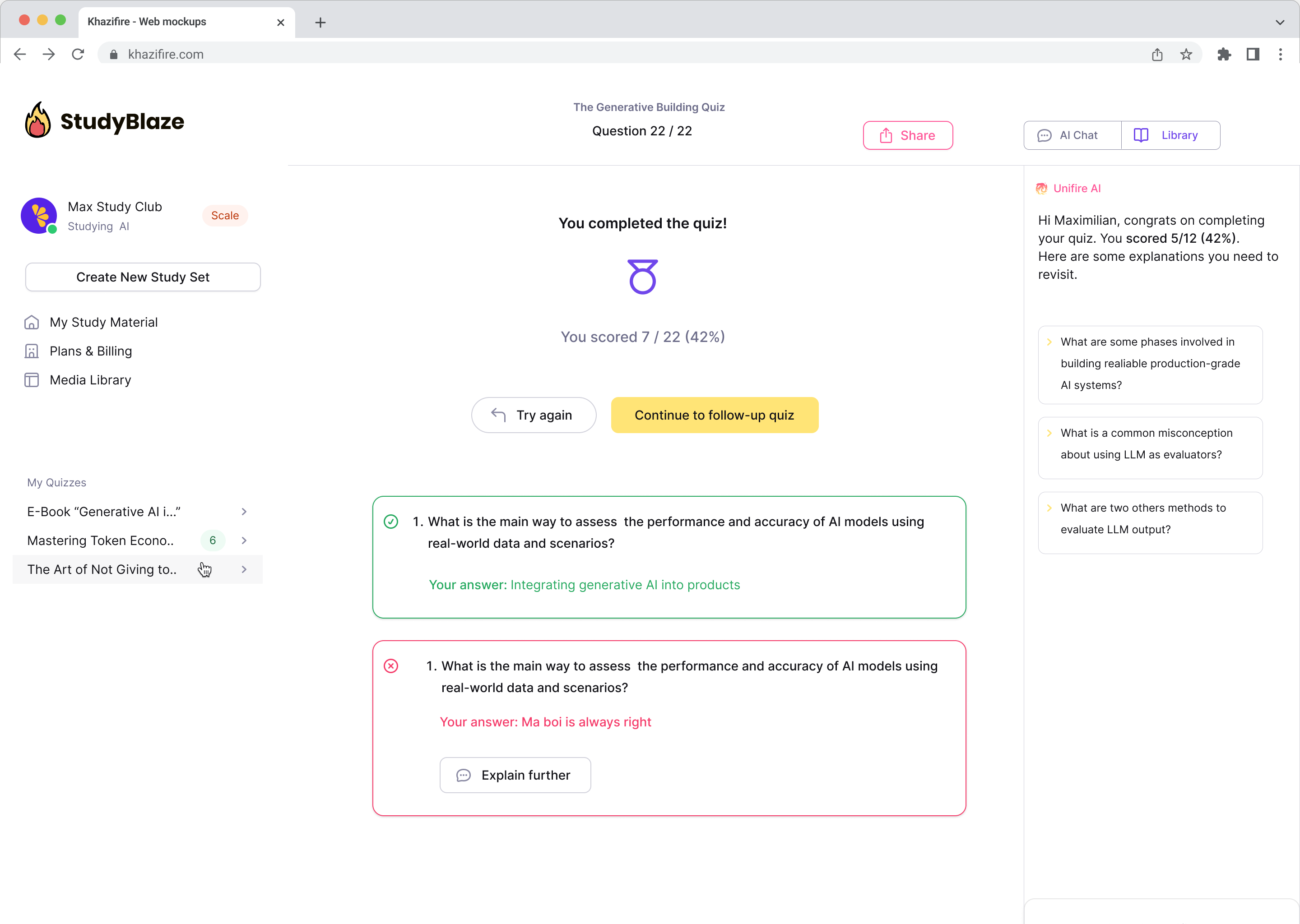
En popüler sorular
Sizin gibi kullanıcıların en önemli sorularına cevap veriyoruz.
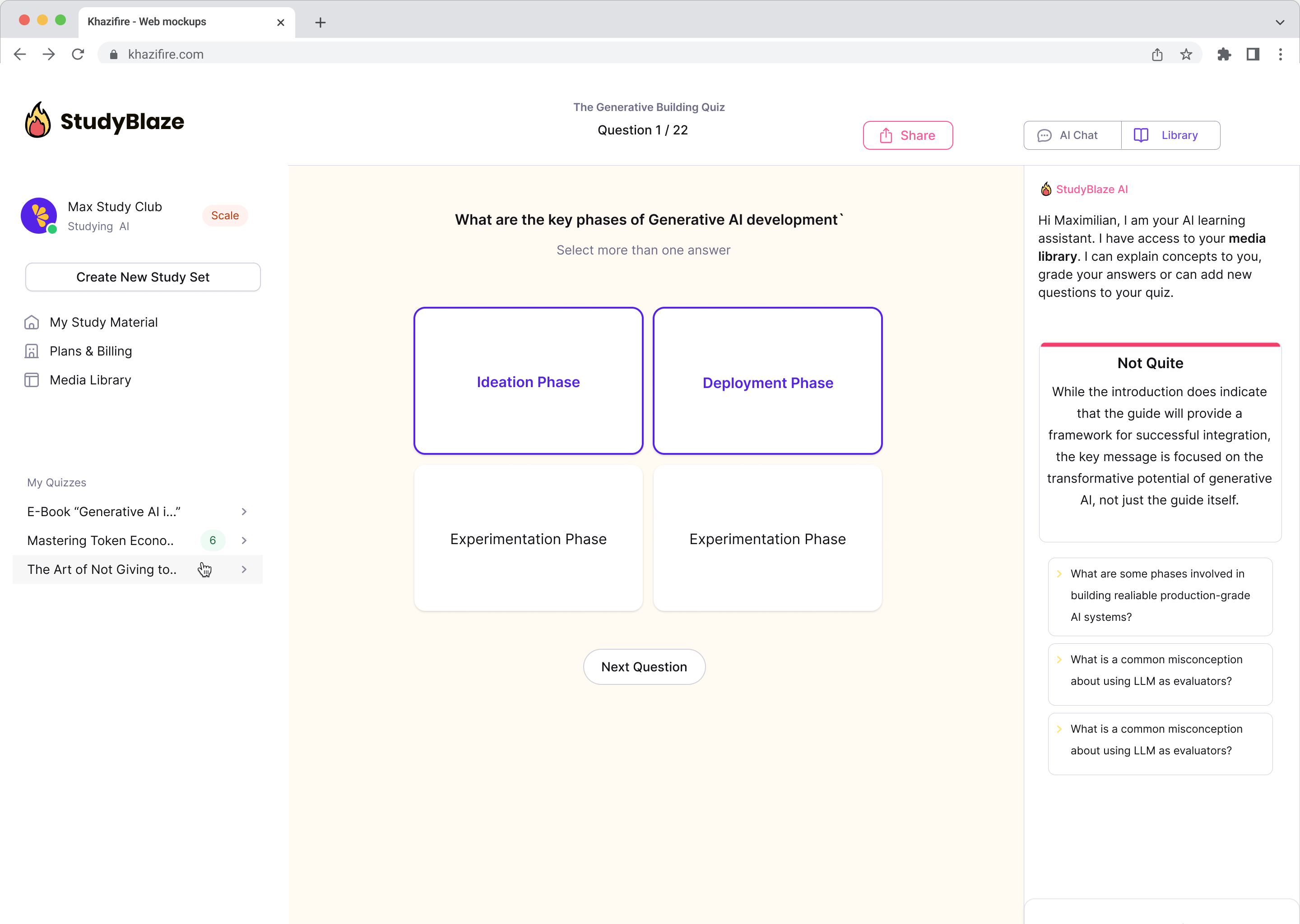
Çalışma alışkanlıklarınızı geliştirin
StudyBlaze ile öğrenme hızınızı hemen artırabilirsiniz. Sıkıcı materyalleri tekrar tekrar okumak yerine, saatlerce manuel bilgi kartı ve özet oluşturma işlemi yapmadan bilginizi daha hızlı test edin.
