Генератор ИИ для
Викторины, карточки
& Больше
Превратите свой скучный учебный контент в интерактивные рабочие листы, тесты, карточки и практические вопросы на базе ИИ одним нажатием кнопки. Загрузите PDF-файлы, документы, аудио и видео сегодня, чтобы начать.
Прекратите ручную работу
Большинство студентов тратят время на неэффективные методы обучения
Вместо того чтобы перечитывать длинные документы или часами вручную создавать карточки и конспекты, мы поможем вам пропустить эти шаги.
Перестаньте тонуть в информации и позвольте нашему ИИ отфильтровать то, что действительно важно. Быстро начните тестировать себя и совершенствуйтесь быстрее.
Очень немногие могут позволить себе личного репетитора. StudyBlaze меняет это навсегда. Интерактивное обучение ускоряет ваш прогресс в 10 раз.
Создание учебных материалов вручную — это время, которое вы могли бы потратить на обучение и тестирование себя. Уменьшите стресс, полностью исключив ручную работу.
Репетитор на базе искусственного интеллекта доступен круглосуточно
Иметь доступ к репетитору каждый день
Получайте мгновенную обратную связь по вашим ответам
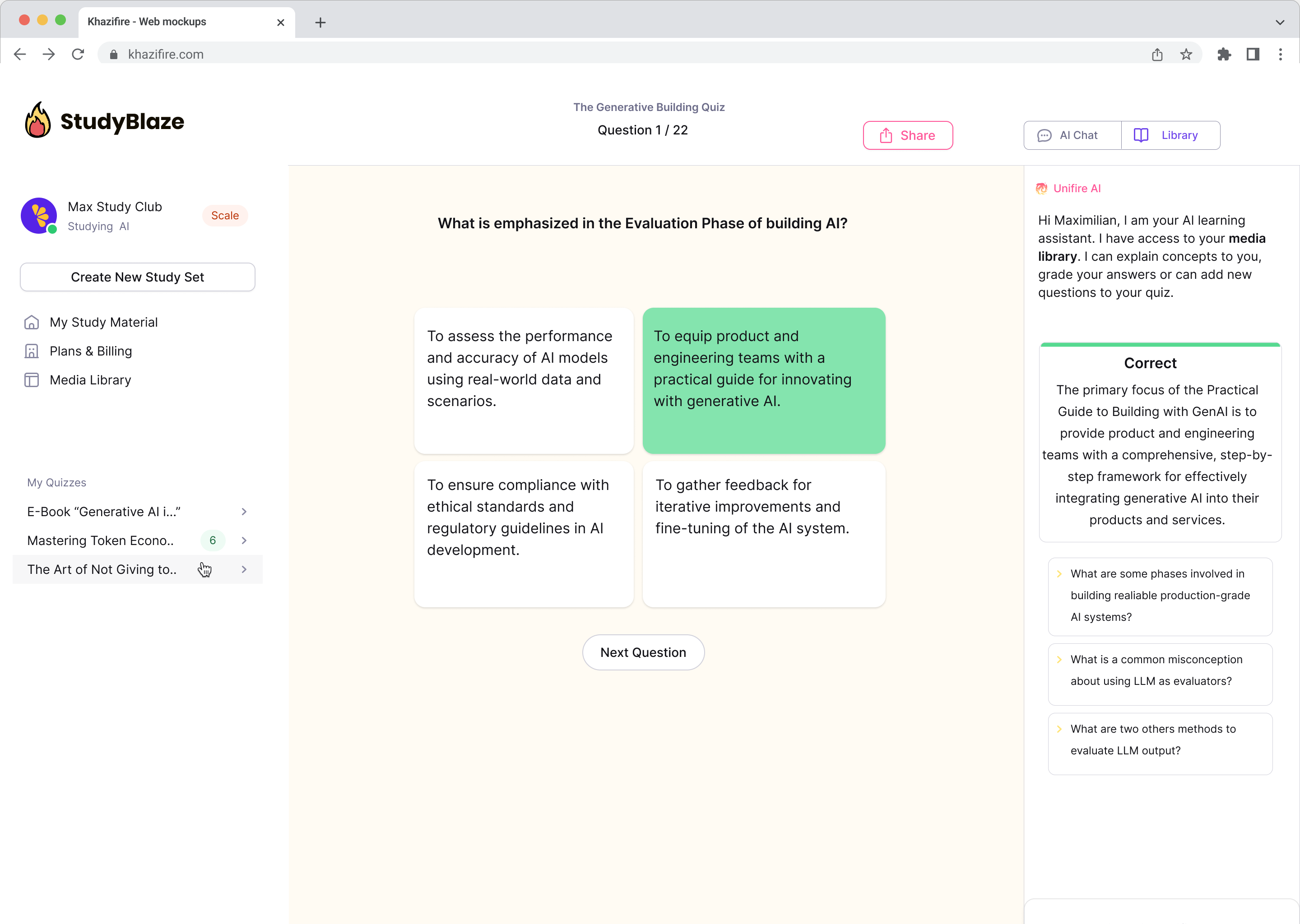
Общайтесь с документами и быстрее разбирайтесь в сложных темах
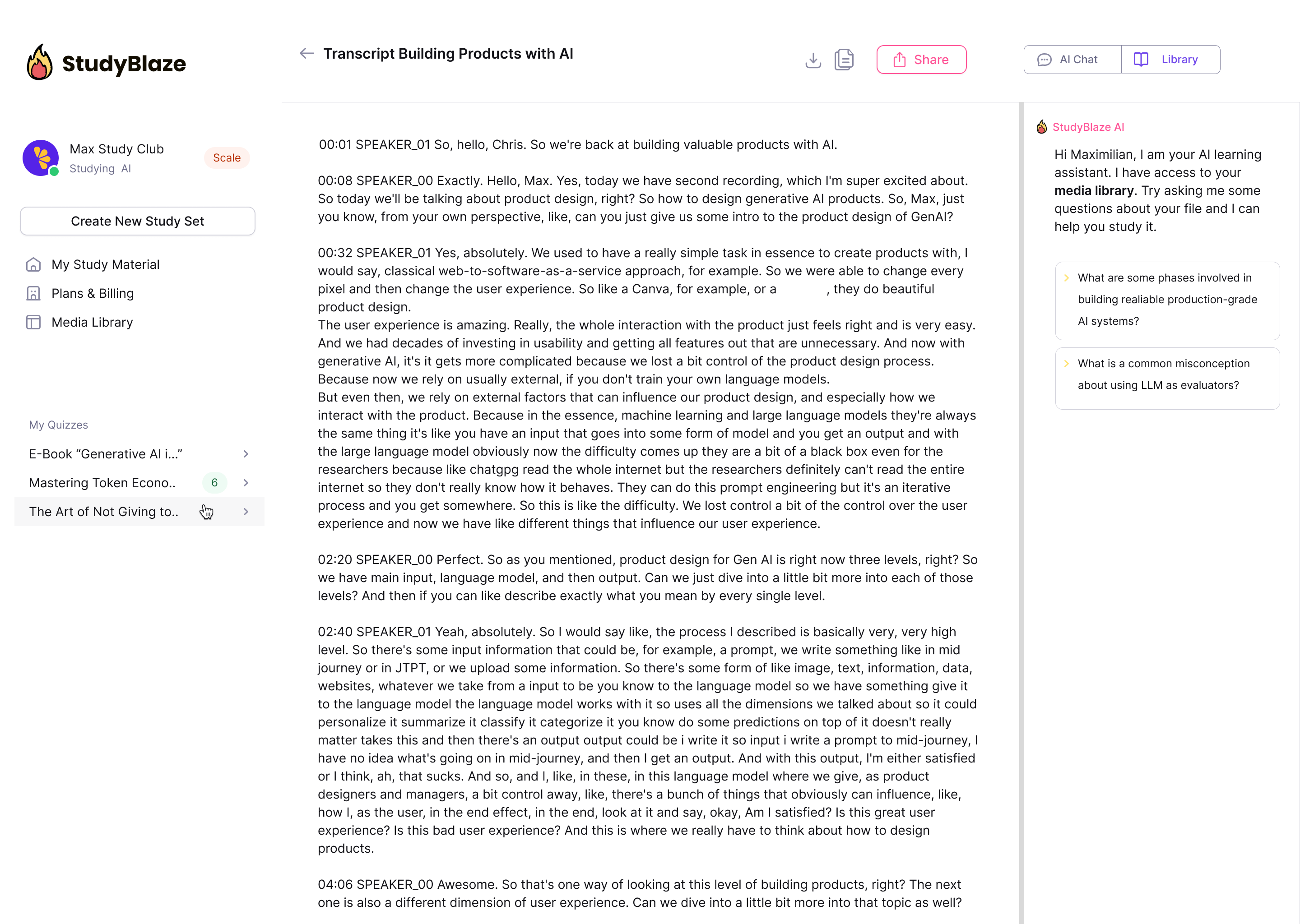
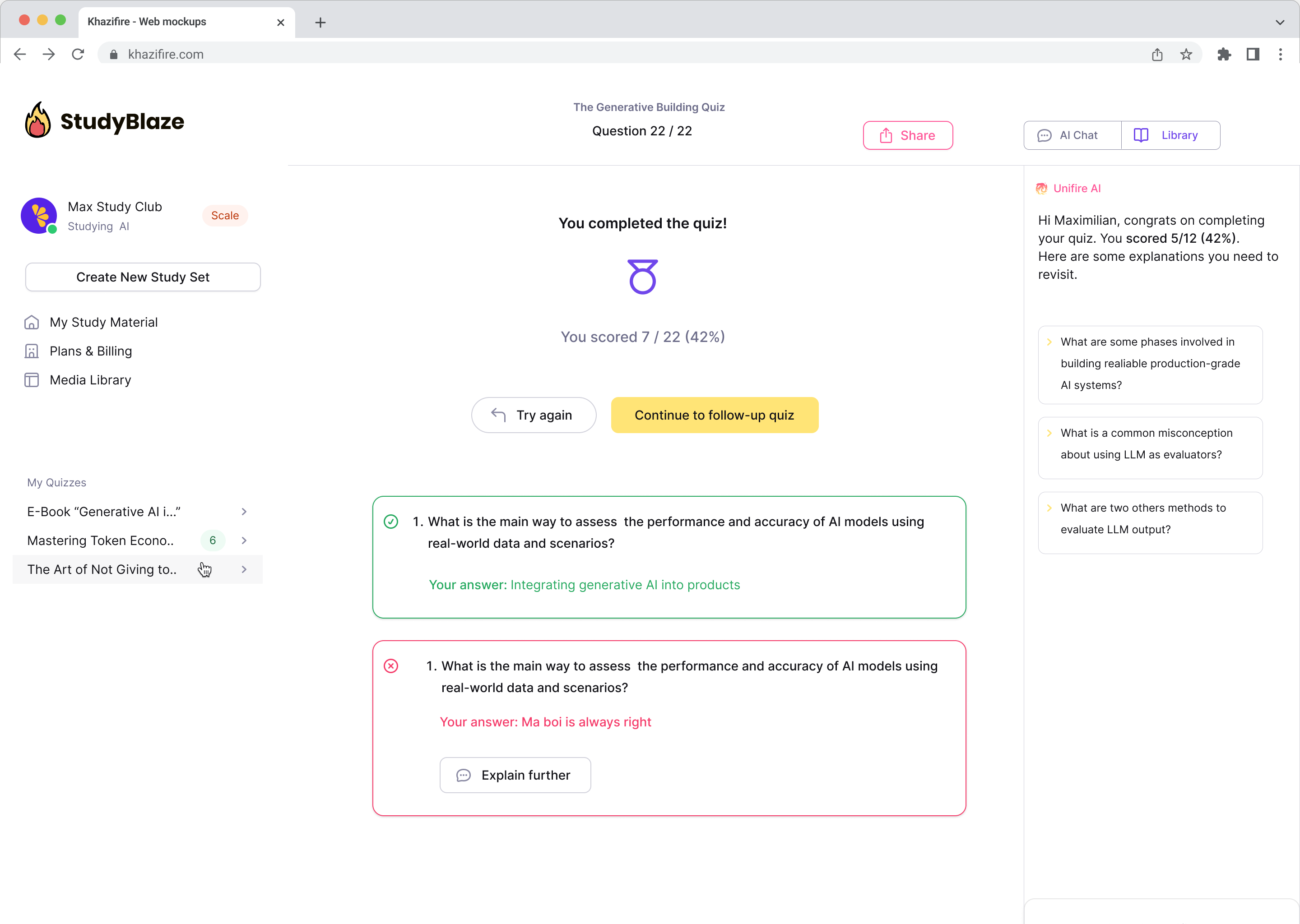
Позвольте вашему ИИ-репетитору оценить ваши ответы и сказать, что вы пропустили
Самые популярные вопросы
Мы отвечаем на самые важные вопросы таких пользователей, как вы.
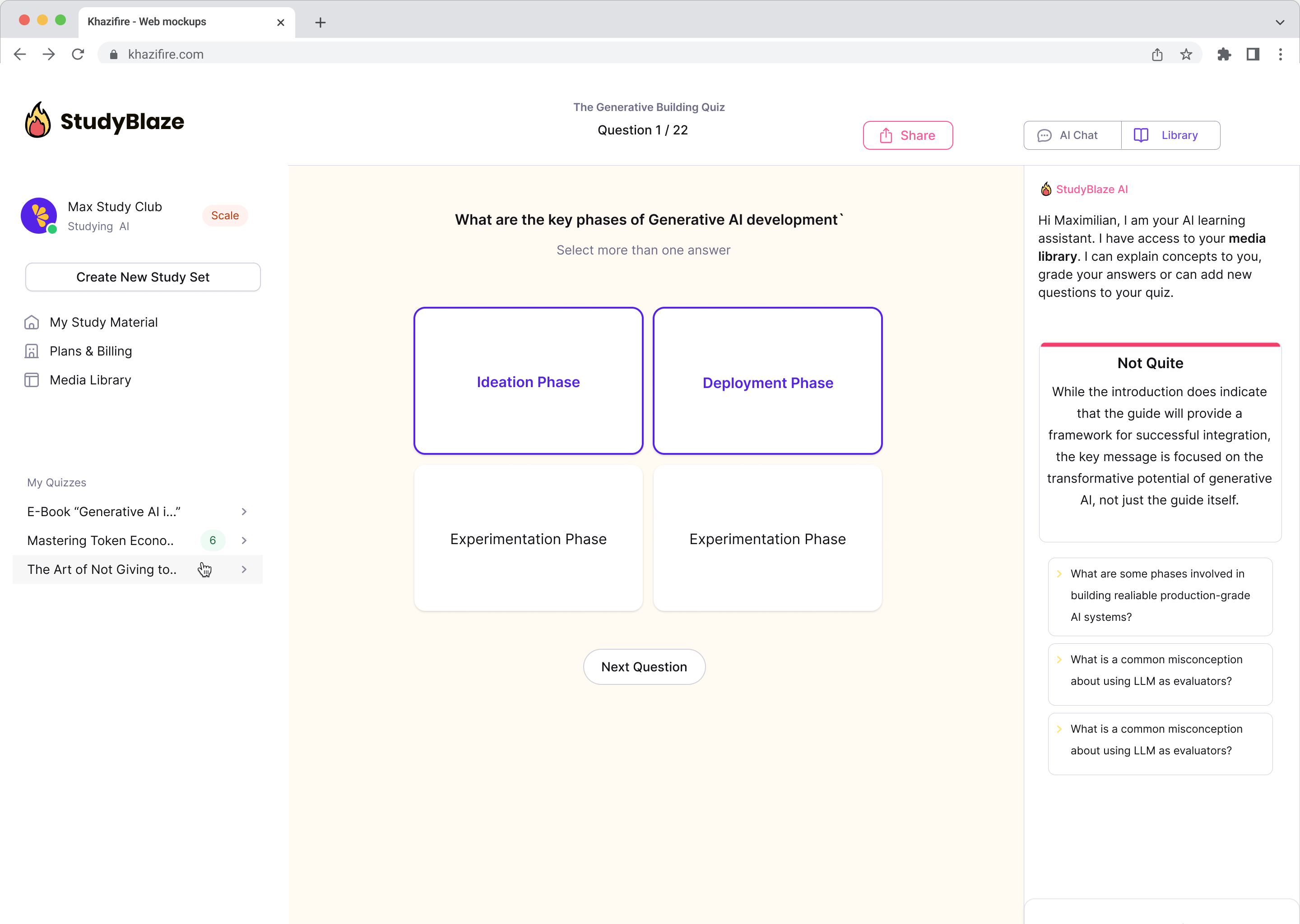
Улучшите свои учебные привычки
С StudyBlaze вы можете немедленно улучшить свою скорость обучения. Вместо того, чтобы читать скучные материалы снова и снова, проверьте свои знания быстрее без часов ручного создания карточек и резюме.
