AI generaator jaoks
Viktoriinid, mälukaardid
& Rohkem
Muutke oma igav õppesisu ühe nupuvajutusega interaktiivseteks tehisintellektiga töölehtedeks, viktoriinideks, mälukaartideks ja harjutusküsimusteks. Alustamiseks laadige üles PDF-id, dokumendid, heli ja video juba täna.
Lõpetage käsitsitöö
Enamik õpilasi raiskab aega ebaefektiivsetele õppemeetoditele
Selle asemel, et pikki dokumente uuesti lugeda või tunde käsitsi mälukaarte ja kokkuvõtteid luua, aitame teil need sammud vahele jätta.
Lõpetage teabesse uppumine ja laske meie tehisintellektil välja filtreerida, mis on tõeliselt oluline. Hakake ennast kiiresti testima ja täiustage end kiiremini.
Väga vähesed inimesed saavad endale lubada isiklikku juhendajat. StudyBlaze muudab seda igaveseks. Interaktiivne õppimine muudab teie edu 10 korda kiiremaks.
Õppematerjalide käsitsi loomine on aeg, mille võiksid kulutada koolitusele ja enda testimisele. Vähendage stressi, välistades täielikult käsitsitöö.
AI juhendaja on saadaval ööpäevaringselt
Juurdepääs juhendaja juurde iga päev
Saate oma vastuste kohta kohe tagasisidet
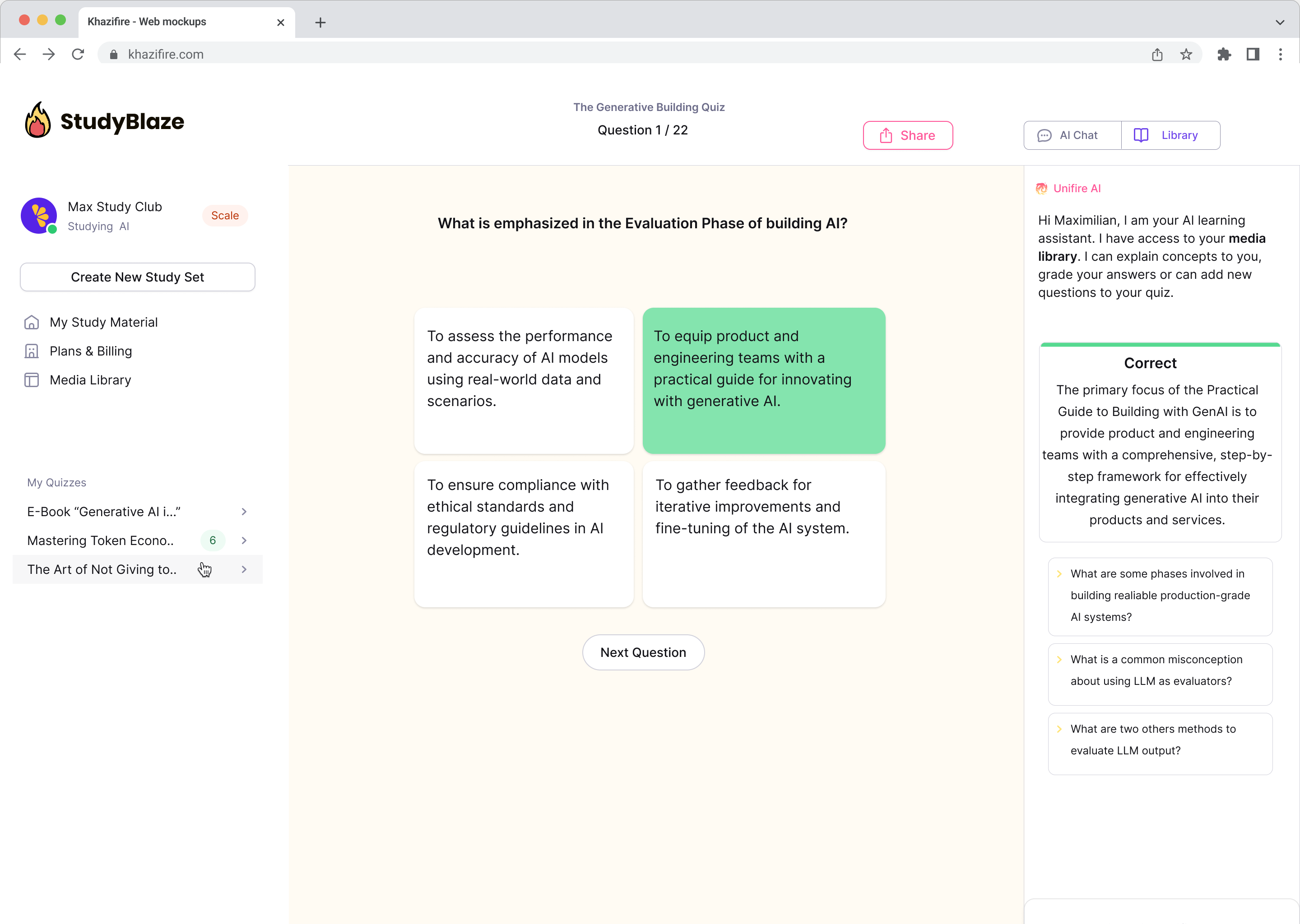
Vestelge oma dokumentidega ja mõistate keerukaid teemasid kiiremini
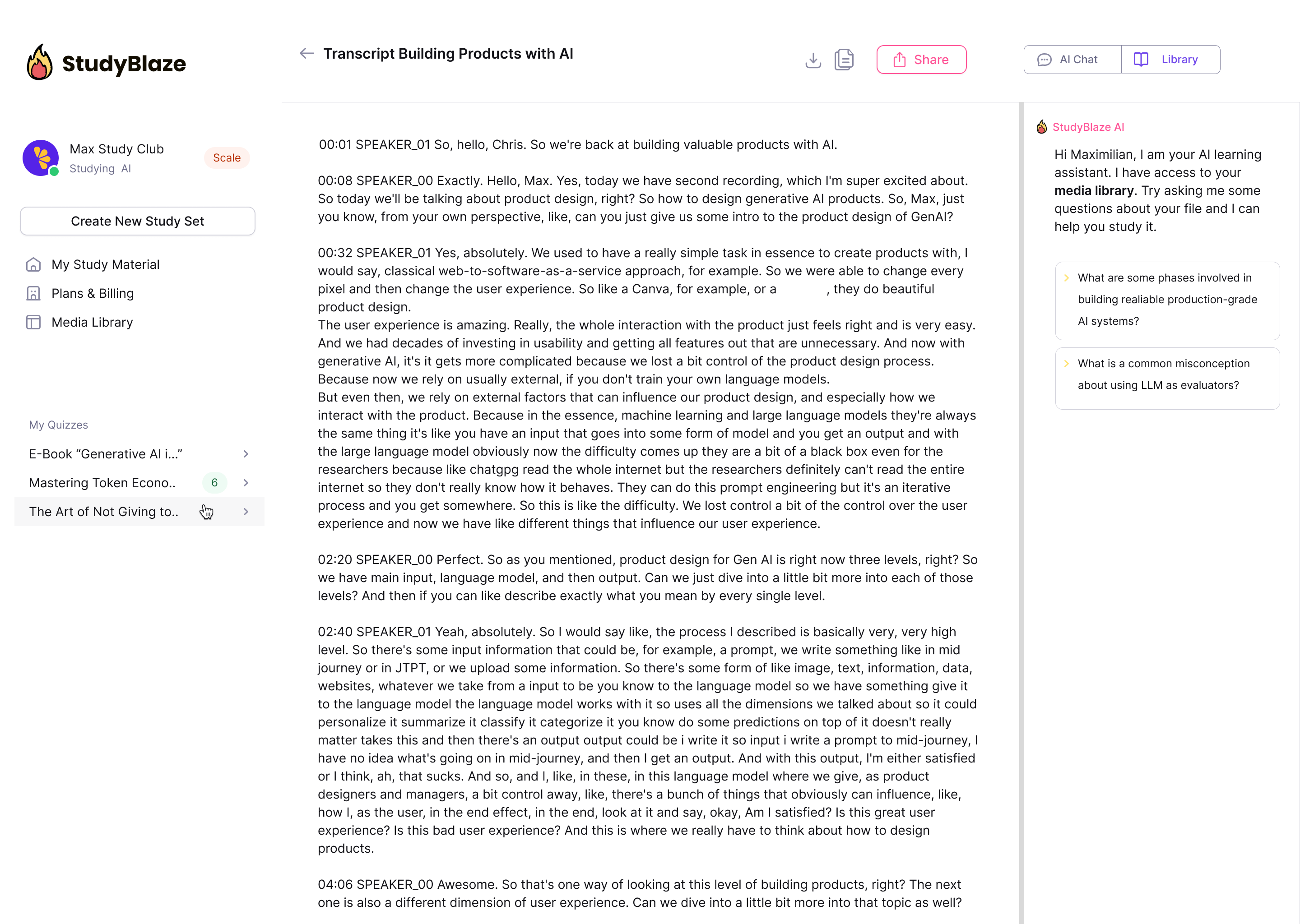
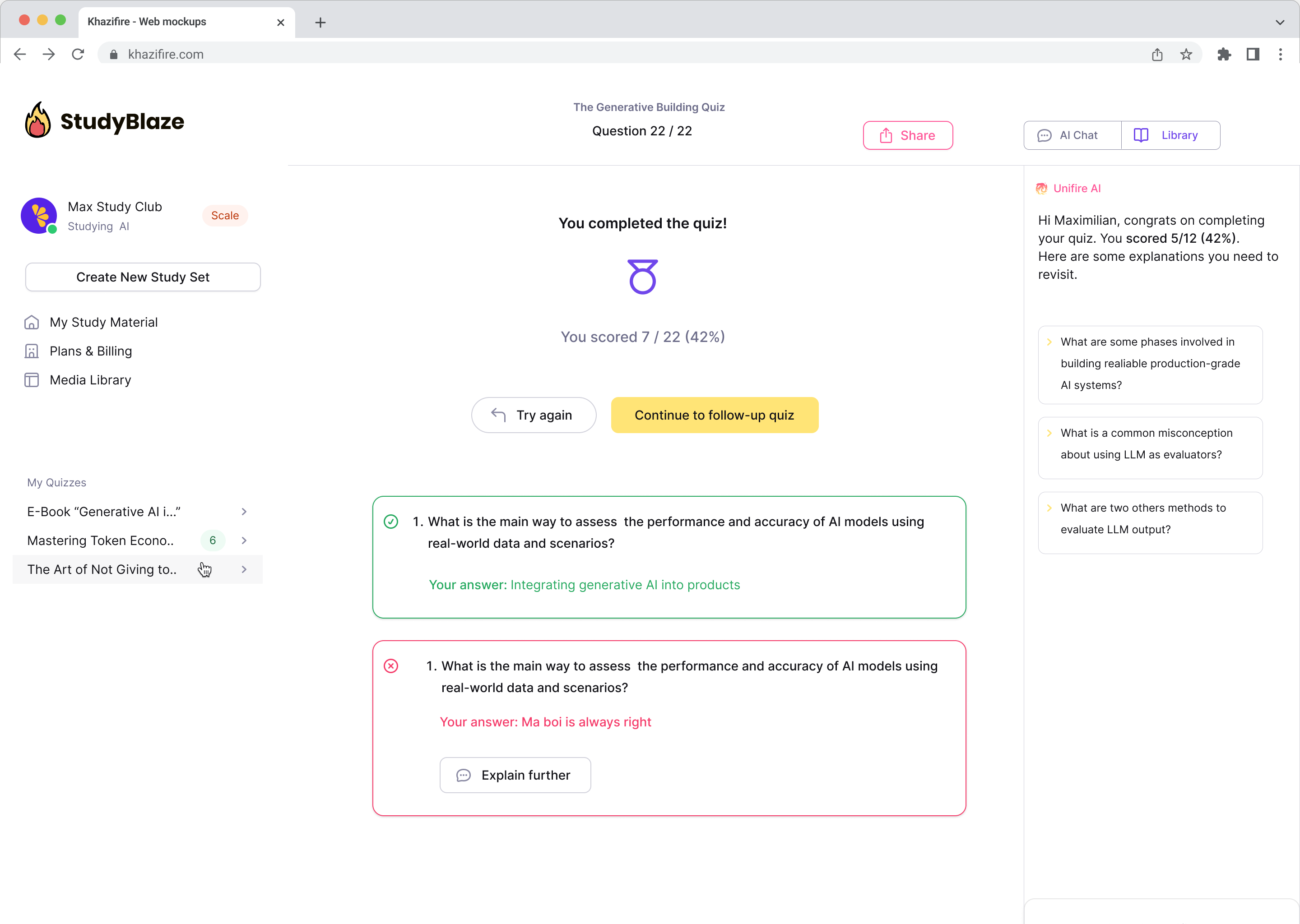
Laske tehisintellekti juhendajal oma vastuseid hinnata ja öelda, millest jäite ilma
Kõige populaarsemad küsimused
Vastame teiesuguste kasutajate kõige olulisematele küsimustele.
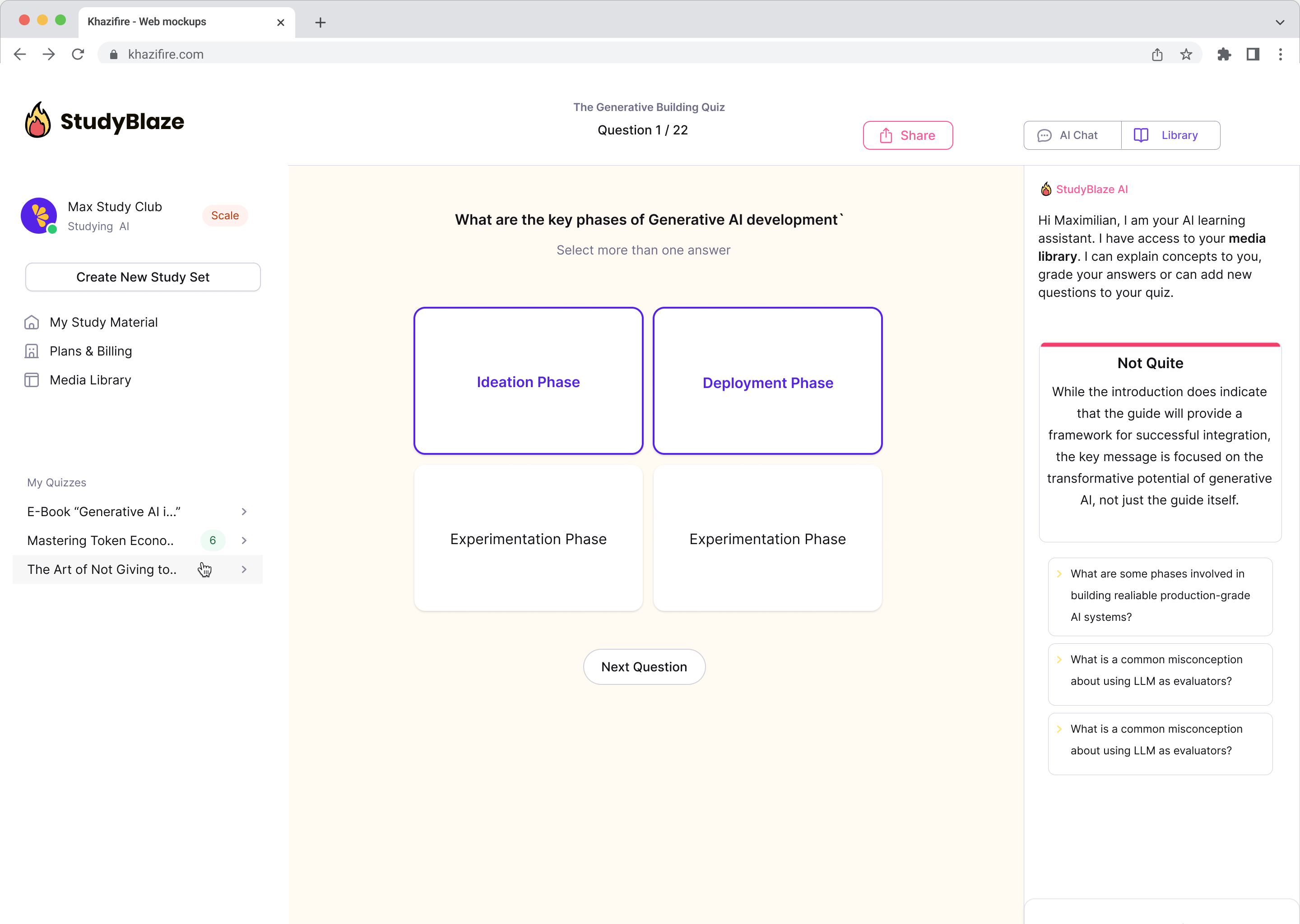
Täiustage oma õppimisharjumusi
StudyBlaze'iga saate kohe oma õppimiskiirust parandada. Selle asemel, et igavaid materjale ikka ja jälle lugeda, pange oma teadmisi kiiremini proovile ilma tundidepikkuse käsitsi välkmälu ja kokkuvõtte loomiseta.
