AI генератор за
Тестове, флаш карти
& Повече ▼
Преобразувайте скучното учебно съдържание в интерактивни работни листове, работещи с изкуствен интелект, тестове, флаш карти и практически въпроси с едно натискане на бутон. Качете PDF файлове, документи, аудио и видео днес, за да започнете.
Спрете ръчната работа
Повечето ученици губят време с неефективни методи на обучение
Вместо да препрочитате дългите си документи или да създавате ръчно флаш карти и резюмета с часове, ние ви помагаме да пропуснете тези стъпки.
Спрете да се давите в информация и оставете нашия AI да филтрира това, което е наистина важно. Бързо започнете да се тествате и се подобрявайте по-бързо.
Много малко хора могат да си позволят личен учител. StudyBlaze променя това завинаги. Интерактивното обучение прави напредъка ви 10 пъти по-бърз.
Ръчното създаване на учебни материали е време, което можете да отделите за обучение и тестване. Намалете стреса, като премахнете изцяло ръчната работа.
Преподавател по изкуствен интелект е на разположение 24/7
Имайте достъп до учител всеки ден
Получавайте незабавна обратна връзка за вашите отговори
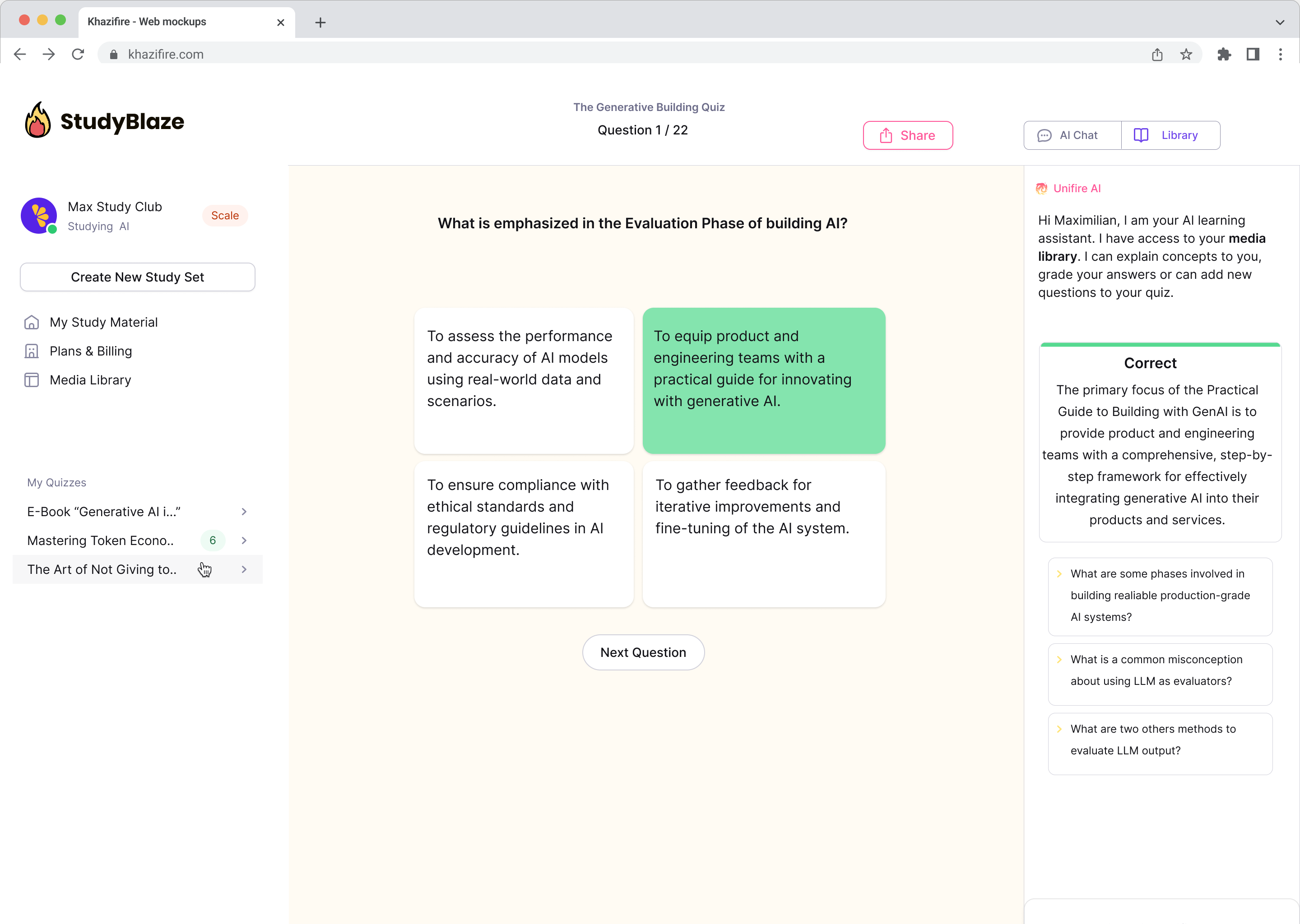
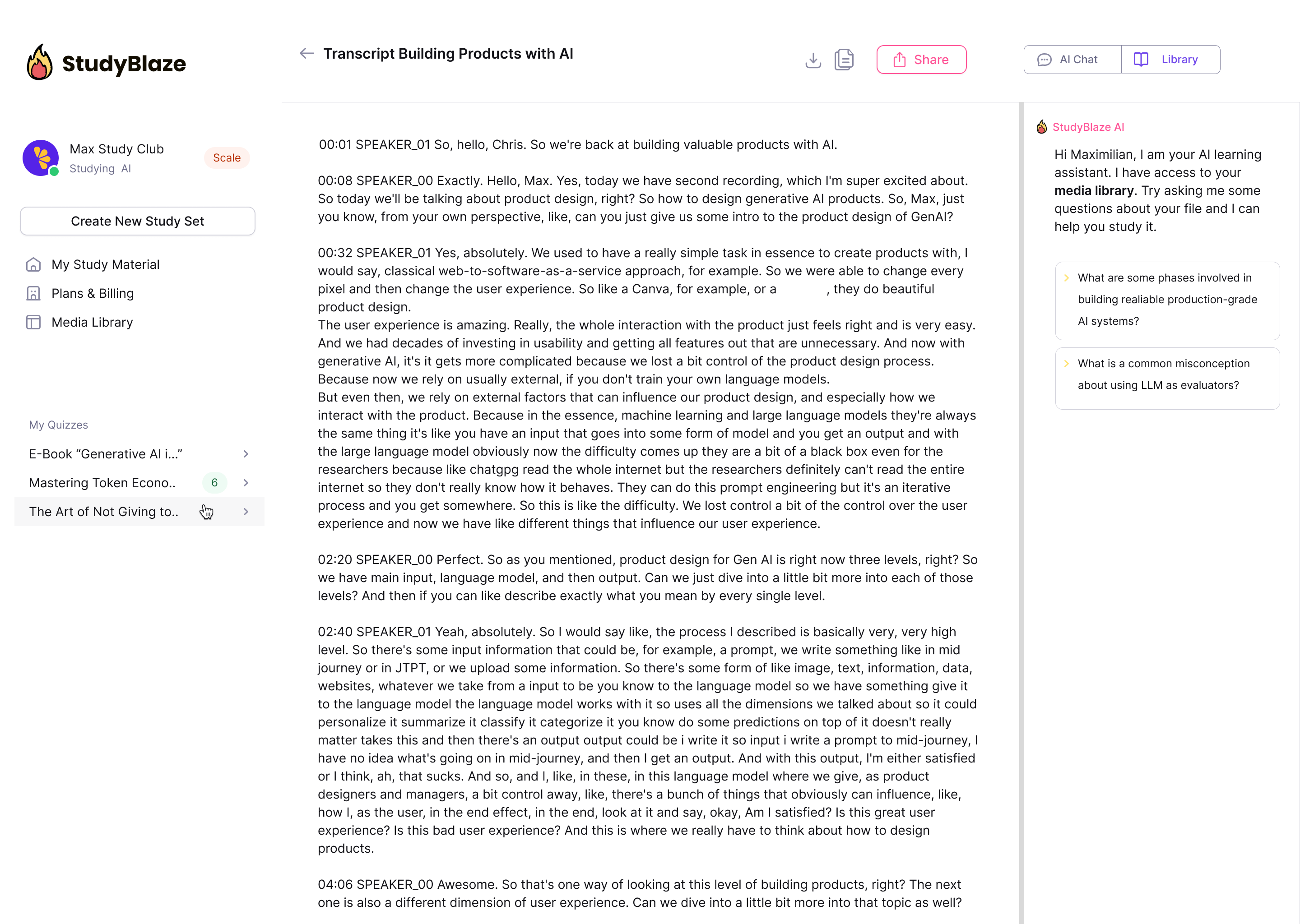
Чатете с вашите документи и разбирайте по-бързо сложни теми
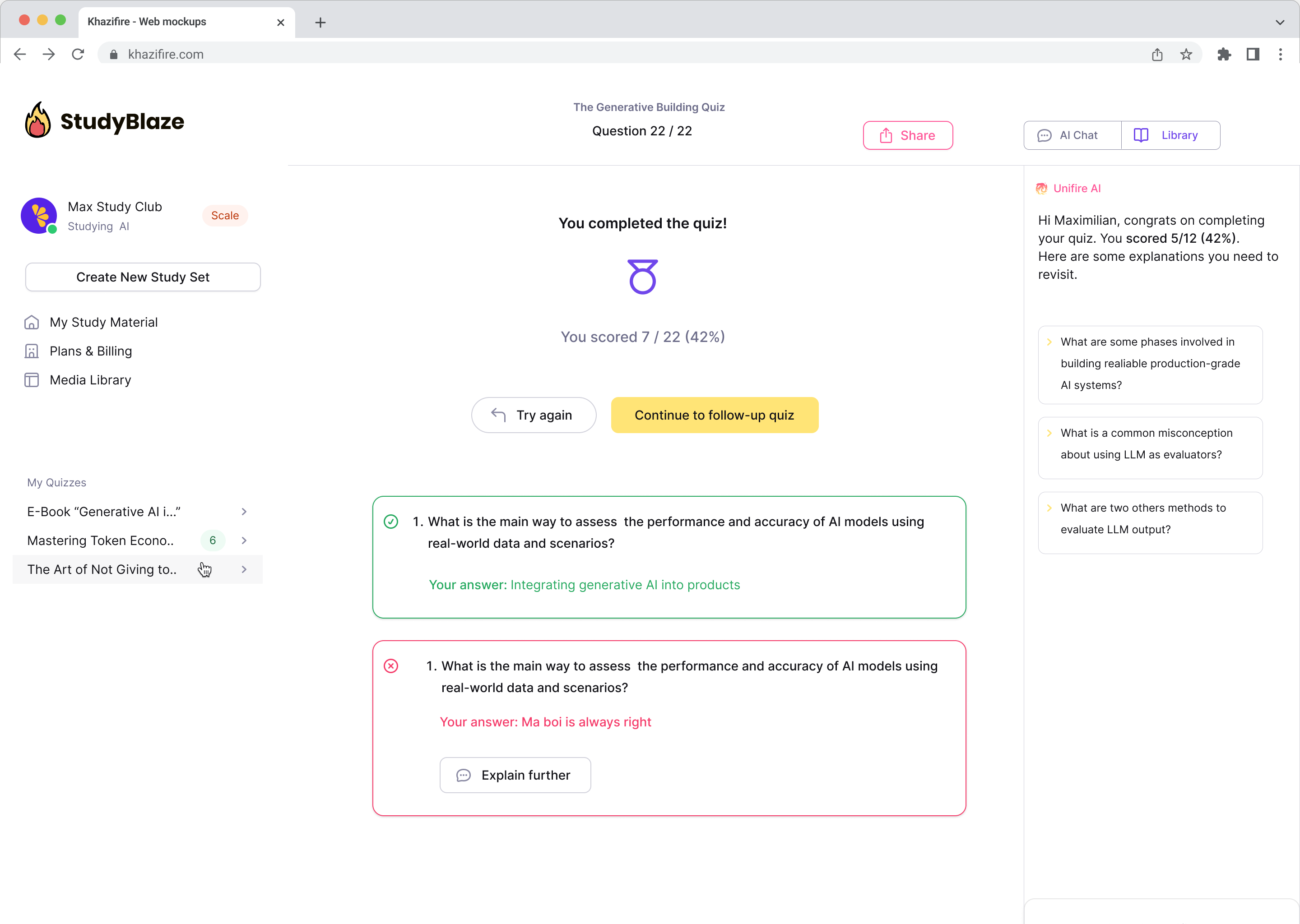
Позволете на вашия преподавател по изкуствен интелект да оцени отговорите ви и да ви каже какво сте пропуснали
Най-популярните въпроси
Ние отговаряме на най-важните въпроси, които имат потребители като вас.
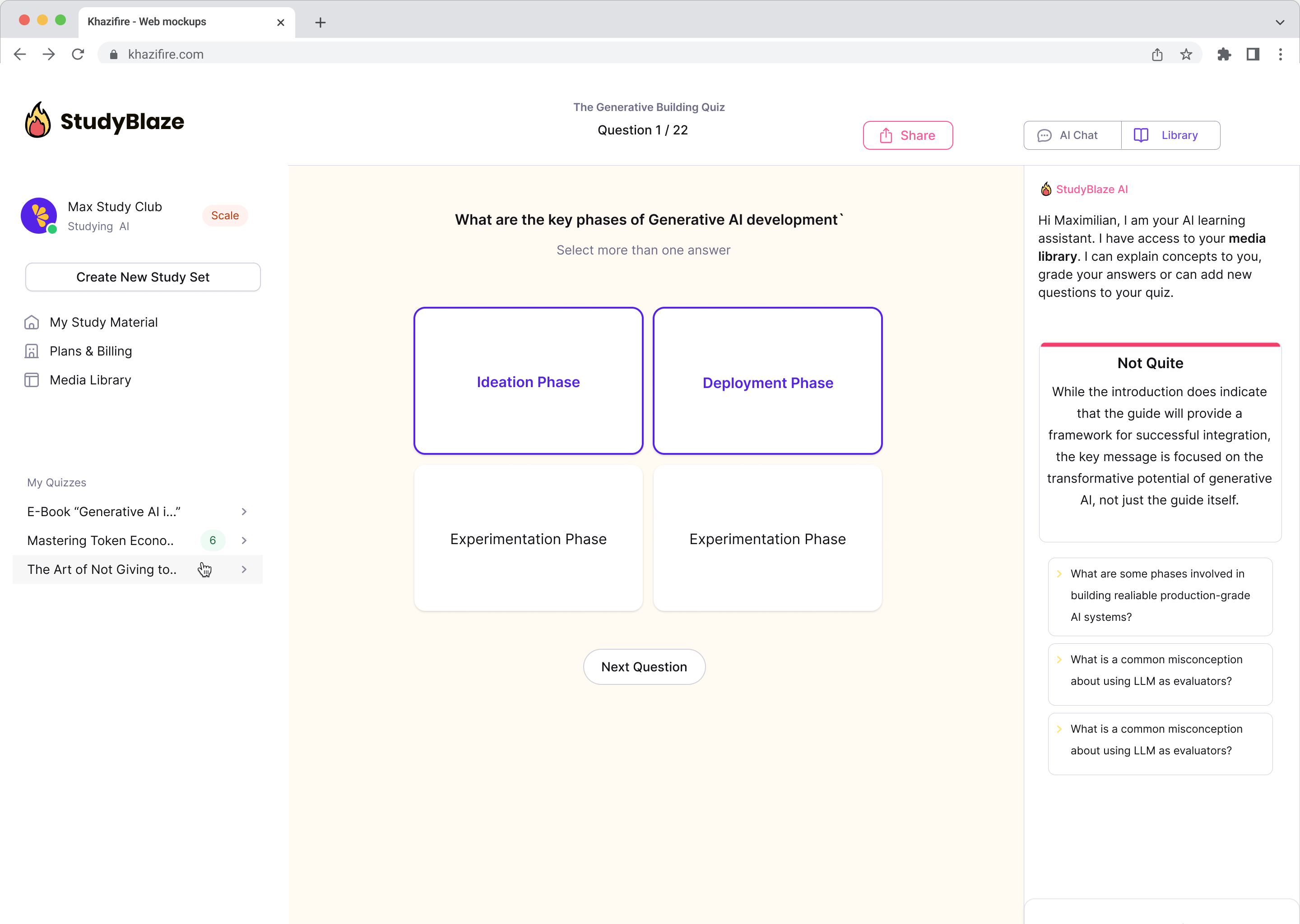
Надградете навиците си за учене
Със StudyBlaze можете незабавно да подобрите скоростта си на обучение. Вместо да четете скучни материали отново и отново, тествайте знанията си по-бързо без часове ръчно създаване на флаш карти и резюме.
